En este momento el mundo está en guerra. Pero esto no es una guerra ordinaria. Es una pelea con un organismo tan pequeño que solo podemos detectarlo mediante el uso de un microscopio, y si no lo detenemos, podría matarnos a millones de nosotros en las próximas décadas. No, no estoy hablando de COVID-19, aunque ese organismo es el que está en la mente de todos en este momento. Estoy hablando de bacterias resistentes a los antibióticos.
Verá, más de 700,000 personas murieron en todo el mundo a causa de infecciones bacterianas el año pasado, 35,000 de ellas en los EE. UU. Si no hacemos nada, ese número podría crecer a 10 millones anuales para 2050, según un informe de las Naciones Unidas.
¿El problema? Uso excesivo de antibióticos en el consultorio del médico o en prácticas ganaderas y agrícolas. Usamos muchas drogas con el tiempo para eliminar todas las bacterias malas, pero solo eliminó la mayoría, no todas, las bacterias malas. Y, como dice la famosa frase de Jeff Goldblum en Jurassic Park, “la vida encuentra un camino”.
Ingrese Felix, una startup de biotecnología en el último lote de Y Combinator que cree que tiene un enfoque novedoso para mantener a raya las infecciones bacterianas: los virus.
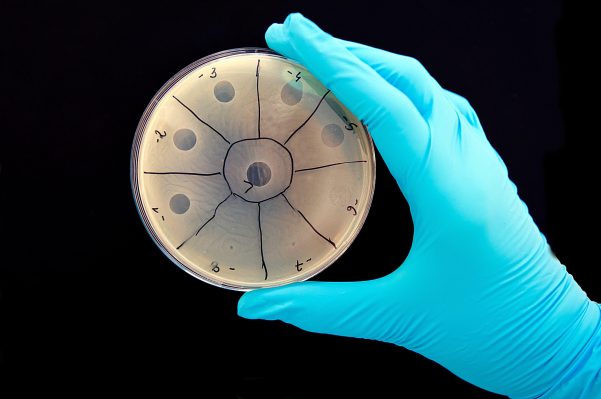
Fago que mata las bacterias en una placa de Petri
Parece extraño en un momento de preocupación generalizada sobre el virus corona el mirar cualquier virus con buena luz, pero como lo explica el cofundador Robert McBride, la tecnología clave de Felix le permite dirigir su virus a sitios específicos en bacterias. Esto no solo mata a las bacterias malas, sino que también puede detener su capacidad de evolucionar y volver a ser resistente.
Pero la idea de usar un virus para matar bacterias no es necesariamente nueva. Los bacteriófagos, o virus que pueden “infectar” bacterias, fueron descubiertos por primera vez por un investigador inglés en 1915 y la terapia de fagos comercializada comenzó en los Estados Unidos en la década de 1940 a través de Eli Lilly and Company. Justo en ese momento aparecieron los antibióticos y los científicos occidentales nunca parecieron explorar más la terapia.
Sin embargo, con muy pocas soluciones nuevas que se ofrecen y el modelo estándar de medicamentos no funciona de manera efectiva para combatir la situación, McBride cree que su compañía puede volver a poner la terapia de fagos a la vanguardia.
Felix ya ha probado su solución en un grupo inicial de 10 personas para demostrar su enfoque.
La investigadora Felix ayuda a la paciente de fibrosis quística Ella Balasa a través de la terapia con fagos
“Podemos desarrollar terapias en menos tiempo y por menos dinero que los antibióticos tradicionales porque apuntamos a indicaciones huérfanas y ya sabemos que nuestra terapia puede funcionar en humanos”, dijo McBride a TechCrunch. “Argumentamos que nuestro enfoque, que vuelve a sensibilizar las bacterias a los antibióticos tradicionales, podría ser una terapia de primera línea”.
Felix planea desplegar su tratamiento en aquellos que sufren de fibrosis quística primero, ya que no hay cura para esta enfermedad, que tiende a requerir un flujo casi constante de antibióticos para combatir las infecciones pulmonares.
El siguiente paso será llevar a cabo un pequeño ensayo clínico con 30 personas, luego, a medida que el modelo de investigación y desarrollo científico tiende a ir, un ensayo humano más grande antes de buscar la aprobación de la FDA. Pero McBride espera que su solución viral se demuestre a tiempo para ayudar al ataque de resistencia a los antibióticos.
“Sabemos que el desafío resistente a los antibióticos es grande ahora y solo va a empeorar”, dijo McBride. “Tenemos una solución tecnológica elegante para este desafío y sabemos que nuestro tratamiento puede funcionar. Queremos contribuir a un futuro en el que estas infecciones no maten a más de 10 millones de personas al año, un futuro que nos entusiasme ”.