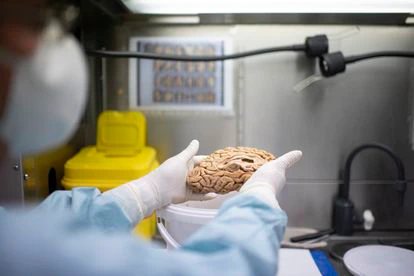
El equipo de la bióloga María Llorens-Martín en el Centro de Biología Molecular Severo Ochoa (CSIC-UAM) había abierto un campo enorme en el estudio del cerebro cuando, hace año y medio, descubrió neuronas inmaduras en el hipocampo de adultos. La investigadora relata que ese hallazgo “sugeriría la existencia de un proceso de neurogénesis, que esas neuronas nacían durante la vida adulta”. El trabajo continuó para descartar que esas células fundamentales para recibir, procesar y transmitir información se hubieran generado al nacer y quedado en estado de inmadurez, como defendían muchos científicos. Ahora, la investigadora y su equipo han demostrado de forma definitiva, tras el estudio de 48 cerebros adultos (15 de ellos cognitivamente sanos), la existencia de células madre e hijas, que se dividen muy rápidamente (proliferativas), maduran y generan nuevas neuronas. Y las deficiencias en este proceso no son la causa de enfermedades neurodegenerativas, sino al revés: son estas dolencias las que limitan la capacidad de seguir creando neuronas. El estudio lo publica este jueves la revista Science.
Llorens-Martin ha cerrado con su descubrimiento una discusión de décadas sobre la neurogénesis en los adultos y ha abierto una enorme puerta al estudio de posibilidades terapéuticas para favorecer el mantenimiento de esta capacidad durante todo el ciclo vital: “Hemos podido reconstruir, por decirlo así, toda la vida de estas nuevas neuronas, desde sus células madre, que las generaron, hasta que se convierten en neuronas maduras. Eso, hasta ahora, no se sabía. Se conocía su presencia, pero no de dónde procedían”.
Según explica la investigadora, “estas células madre proceden del hipocampo, la misma zona donde se encontraron las neuronas inmaduras. Es un área que se denomina giro dentado”. Para identificarlas, se habían utilizado distintos marcadores que podían identificar células madre, pero también astrocitos (células gliales), porque no eran específicos. El estudio de Llorens-Martín ha utilizado una metodología especial para visualizar las células madre neurogénicas y una combinación de marcadores que excluyen que esas puedan ser astrocitos.
La presencia de procesos patológicos que se dan en las enfermedades neurodegenerativas dañan el nicho neurogénico, que se convierte en un entorno hostil para la generación de nuevas neuronas, pierde esa capacidad que en principio debería permanecer de por vida
María Llorens-Martín, Centro de Biología Molecular Severo Ochoa (CSIC-UAM)
La nueva técnica ha permitido observar morfológicamente las células dentro del giro dentado y sus deficiencias. Estos defectos en la neurogénesis, según el estudio, no son la causa de enfermedades como Huntington, párkinson, demencia con cuerpos de Lewy y demencia frontotemporal, sino que pueden ser la consecuencia de estas dolencias. “En el caso de la ELA [esclerosis lateral amiotrófica] se ven afectadas motoneuronas y en el caso del párkinson, neuronas de la sustancia negra. Están muy lejos del hipocampo y, por lo tanto, no podemos decir que estos defectos en neurogénesis sean la causa de estas enfermedades”.
Al contrario, es el hipocampo el que presenta una notable vulnerabilidad a patologías neurodegenerativas. “Cada una de estas enfermedades genera una firma celular propia y daña de manera más acusada a determinadas subpoblaciones celulares que forman parte del proceso de neurogénesis hipocampal adulta. De esta manera, algunas poblaciones celulares son más vulnerables a determinadas enfermedades que a otras”, explican los autores de la investigación.

Llorens-Martín considera que las deficiencias en la neurogénesis adulta “pueden estar relacionadas con los síntomas cognitivos, con la alteración del estado de ánimo o los procesos depresivos que muchas veces ocurren estos pacientes”. “La presencia de estos procesos patológicos que se dan en las enfermedades neurodegenerativas”, explica, “dañan el entorno, lo que llamamos el nicho neurogénico, que es otra de las cosas que hemos descubierto. Ese nicho se convierte en un entorno hostil, por decirlo así, para la generación de nuevas neuronas, pierde esa capacidad que en principio debería permanecer de por vida. Vemos neurogénesis en los pacientes con todas estas enfermedades y en todas las etapas. Sin embargo, vemos alteraciones en el número, menos proliferación, lo cual nos habla de que estas células están más inactivas. Y una característica común a todas las enfermedades son las alteraciones en la maduración de las nuevas neuronas, es decir, que aunque haya más, no maduran correctamente, tienen una forma que llamamos aberrante y lo más probable es que mueran por el camino, pero la microglía, como sistema inmune del cerebro, no es capaz de eliminarlas”.
La demostración de la neurogénesis adulta, la localización de su origen y los efectos de las enfermedades sobre este proceso revelan nuevas opciones terapéuticas de gran importancia. “Nuestro estudio”, asegura Llorens-Martín, “permite abrir una puerta a la posibilidad de recuperar la neurogénesis y atenuar algunos de los efectos colaterales de las enfermedades que están directa o quizás indirectamente relacionadas con el hipocampo, es decir, todas aquellas funciones en las cuales participan estas nuevas neuronas que no sean motoras”. “Recuperando esta neurogénesis”, añade, “podríamos o bien prevenir la aparición de estos déficits o quizás ralentizar su progresivo avance. Y también existe un campo terapéutico para favorecer la neurogénesis. Hay algunos estudios en marcha sobre los efectos de determinadas estrategias, principalmente no farmacológicas, en ratones. Nuestro grupo se lleva bastantes años en intentando revertir las alteraciones cognitivas y celulares que se producen en modelos animales mediante, por ejemplo, ejercicio físico o lo que denominamos enriquecimiento ambiental, que es una combinación un poco más compleja y que engloba, además de ejercicio físico, estimulación cognitiva y una mayor interacción social. Hay un consenso generalizado de que, cuando empiezan a aplicarse antes de la aparición de la enfermedad, sí que son efectivas”.
Jesús Ávila, investigador del Centro de Biología Molecular Severo Ochoa, considera el descubrimiento un “hito” que cierra una gran controversia sobre la neurogénesis en adultos: “Este proceso disminuye, pero existe en las personas mayores, aunque se ve afectado por enfermedades degenerativas”. “Es muy relevante”, añade el científico, “el concepto de prevención que aporta la investigación, ya que, en muchos casos, la diagnosis clínica de la enfermedad llega demasiado tarde, cuando ya han muerto muchas neuronas y es difícil arreglar algo que ya está destruido”. Ávila destaca que la investigación permite buscar “qué es lo acontece antes, cuáles son los riesgos y si están relacionados con el modo de vida en los años anteriores de la vejez o con un estrés crónico”.
El científico considera que el estudio aporta una nueva forma de aproximarse a las enfermedades neurodegenerativas: “Se habla de ellas como si fuera un conjunto, pero es necesario buscar especificidades y las zonas afectadas. El trabajo de Llorens-Martín abre un nuevo camino”.
Puedes seguir a MATERIA en Facebook, Twitter e Instagram, o apuntarte aquí para recibir nuestra newsletter semanal.
