- Las enfermedades de la retina y la degeneración relacionada con la edad pueden provocar problemas de visión.
- Los científicos que trabajan para restaurar la vista están desarrollando múltiples soluciones prometedoras.
- Estas técnicas pasan por alto las retinas dañadas con una variedad de enfoques alternativos que convencen al cerebro para que vea.
La retina humana, la parte del cerebro sensible a la luz situada en la parte posterior del ojo, es una hazaña de ingeniería en el corazón de un sentido crítico: la vista. Por lo tanto, las enfermedades de la retina como la retina pigmentosa o la degeneración macular relacionada con la edad, que provocan problemas de visión y ceguera, pueden ser particularmente intratables y devastadoras.
Pero los científicos se están concentrando en un conjunto de estrategias que pueden ofrecer un rayo de esperanza.
👁 Las nuevas tecnologías son increíbles. Vamos a nerd sobre ellos juntos.
Exquisitamente organizada, la retina detecta la luz del entorno que nos rodea y la transforma en señales electroquímicas que finalmente llegan a la corteza visual del cerebro, donde se procesan e interpretan en imágenes que podemos entender. Pero el daño a cualquier parte del sistema, desde los fotorreceptores sensibles a la luz hasta las células bipolares con las que se comunican y las células ganglionares que transmiten esta información a través del nervio óptico al cerebro, puede afectar nuestra visión.
Si bien existen innumerables estrategias para restaurar la vista, las prótesis retinianas o los conjuntos de electrodos implantados en la retina son los que más han avanzado. Sin pasar por los fotorreceptores dañados, los electrodos estimulan directamente las neuronas sobrevivientes, ya sean células bipolares o ganglionares, que alimentan la corteza visual del cerebro, impartiendo una versión artificial de la vista a los pacientes. La mayoría de las configuraciones incluyen una cámara montada en anteojos que capta imágenes, que se traducen en señales eléctricas mediante un procesador. Estas señales se envían luego a los conjuntos de electrodos.
Sin embargo, las tecnologías actuales no pueden replicar las actividades de la retina, que es un microprocesador complejo con múltiples etapas sinápticas, que condensa información de 120 millones de fotorreceptores a 1,2 millones de células ganglionares, dice Diego Ghezzi, profesor de neuroingeniería en la Ecole Polytechnique Fédérale. de Lausana en Suiza. Y se desconoce la salida exacta de la retina al cerebro, los patrones espaciotemporales de pulsos eléctricos generados por las células ganglionares. “Entonces, dado que no tenemos tecnología que pueda reproducir perfectamente este código individualmente en 1,2 millones de células ganglionares de la retina, lo que hacemos es una aproximación”, dice Ghezzi. Mecánica Popular.
Una prótesis para el ojo
El equipo de Ghezzi ha ideado una prótesis de retina fotovoltaica, que funciona de manera similar a la Argo II, la prótesis ahora descontinuada que había estado en uso desde 2011. “La gran diferencia es que nuestros electrodos, como los paneles solares, son capaces de absorber la luz y convertirla en electricidad dentro del dispositivo”, dice Ghezzi. Y aunque las gafas, que amplifican la luz ambiental a una intensidad que la prótesis puede detectar, siguen siendo necesarias, el sistema de Ghezzi viene con varias mejoras con respecto a las tecnologías anteriores.
“La agudeza visual está limitada por la distancia entre los electrodos”, dice Ghezzi. “En nuestro dispositivoesa distancia es de 120 micras [compared to 575 microns in the Argus II], que corresponde a una agudeza visual de 20/480.” Sin embargo, trucos adicionales pueden aumentar este número. “Puede hacer zoom con las gafas, por lo que si tiene que mirar cosas muy pequeñas como la página de un libro de texto, el zoom puede aumentar su resolución de 20/400 a 20/200, por ejemplo”. Pero este truco se realiza a costa de cortar el campo visual, o el área que es visible cuando fijas la mirada.
Experimentos y simulaciones han demostrado que un ángulo visual de al menos 30 grados es necesario para la movilidad funcional, o la capacidad de moverse con seguridad a través de un entorno. El objetivo de Ghezzi, por lo tanto, era “tener una agudeza visual lo suficientemente buena junto con un ángulo visual muy grande”.
Compuesta por 10.498 píxeles y cubriendo un ángulo visual de 43 grados, la prótesis de su equipo representa una notable mejora con respecto a los 20 grados logrados por el Argus II; y debido a que está construido con polímeros orgánicos flexibles, se ajusta naturalmente a la superficie curva del ojo. Los investigadores probaron recientemente el dispositivo en Mini cerdos de Göttingen, demostrando que las prótesis implantadas responden a la luz. El próximo paso, dice Ghezzi, es probar el implante en humanos.
Ondas de sonido que pueden estimular la visión
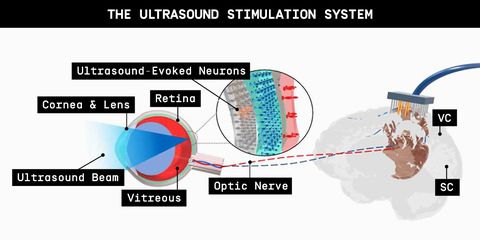
Otros científicos, como Qifa Zhou de la Universidad del Sur de California, han abordado el problema desde una perspectiva diferente. En lugar de estimular las neuronas retinianas desde el interior de la retina, Zhou y sus colegas activaron su actividad con ultrasonido u ondas sonoras de alta frecuencia que se originan fuera del ojo.
“Con la estimulación eléctrica, los cirujanos deben colocar los electrodos dentro del ojo; es una tecnología invasiva”, dice Zhou Mecánica Popular. “Nuestro método es potencialmente menos riesgoso”. Al igual que otras prótesis de retina, la configuración de Zhou incorporaría una cámara que recibe imágenes y las procesa en un patrón, en este caso, ondas de ultrasonido, que se transmite al ojo. Prueba de concepto los estudios con ratas relacionaron la estimulación de ultrasonido de la retina con respuestas eléctricas en los centros visuales del cerebro.
Una solución viral
Varios grupos buscan la restauración de la visión a través de la optogenética, en la que se induce a las neuronas de la retina, a través de un virus que se dirige a células específicas, a expresar proteínas sensibles a la luz en sus membranas celulares. José-Alain Sahel y sus colegas fueron los primeros en implementar con éxito esta técnica en pacientes, según informaron en un artículo publicado el año pasado.
Aunque su método también requiere una cámara y un procesador para traducir las imágenes del entorno en pulsos de luz que pueden excitar las neuronas transformadas, es probable que sea más confiable y versátil que las prótesis tradicionales. Las células de la retina continúan expresando la proteína fotosensible después de una inyección única del virus, mientras que los implantes físicos podrían degradarse y dejar de funcionar, lo que conlleva riesgos de infección. “Y las gafas, dado que están fuera de los ojos, pueden evolucionar con el tiempo”, dice Sahel, presidente de Oftalmología de la Facultad de medicina de la Universidad de Pittsburgh y director del UPMC Eye Center. Mecánica Popular. “Ya son diferentes de las primeras gafas que desarrollamos, con más por venir”.
Pero, de hecho, ¿qué ven los pacientes?
“El tipo de señal que se produce con este [light-sensitive] la proteína es un nuevo tipo de señal y el paciente tiene que aprender a entenderla”, dice Sahel, comparando el proceso con el aprendizaje de un idioma extranjero. Cada píxel de la cámara reacciona a un cambio de luz, por lo que es como mirar una pantalla centelleante, donde los píxeles parpadean cuando la luz cambia en esa posición. Esta cámara neuromórfica, señala Sahel, está diseñada para imitar parcialmente cómo responde la retina a la luz.
Las señales surgen, por tanto, cuando el objeto se mueve o el paciente mueve la cabeza o los ojos en una especie de detección de bordes, explica Sahel. Gradualmente, los pacientes pueden discernir formas, fuentes de luz, bordes y objetos en movimiento. Dan Dunfee, un paciente que participa en el ensayo clínico en Pittsburgh, dice que es como mirar a través de unos anteojos untados con vaselina a un mundo bañado en diferentes intensidades de azul.
“Veo contraste y luz y los bordes donde el contraste y la luz cambian”, dice Dunfee. Mecánica Popular. “Y cuando encuentro lo que creo que es un borde de algo, busco alrededor para encontrar los otros bordes y, a partir de eso, tengo una idea del tamaño, la forma y cuán reflectante es un objeto”.
La visión que resulta de estas terapias se desvía tanto de la visión natural porque la retina responde a la luz de una manera diferente a como lo hace normalmente, dice Stuart Trenholm, profesor asistente de neurociencia en el Instituto Neurológico de Montreal.
Las células madre tienen el potencial de restaurar la visión
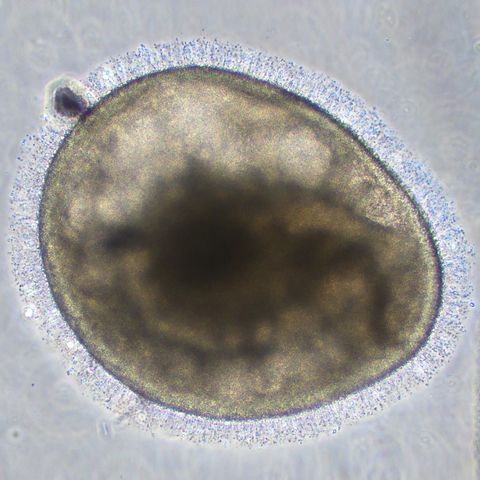
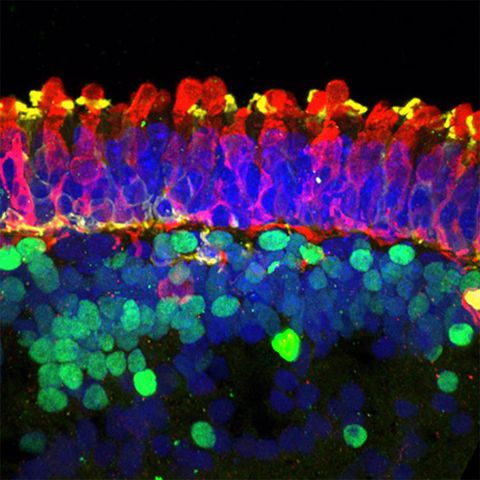
Ahí es donde las terapias con células madre, en las que las propias células del cuerpo pueden ser persuadidas para diferenciarse en células de la retina o incluso en una retina completa, son muy prometedoras. “Casi como por arte de magia, la retina en un plato, o un organoide retinal, parece hacer crecer todas las diferentes partes de la retina”, dice Trenholm. Mecánica Popular. “Y dado que gran parte del desarrollo del cerebro depende del entorno que lo rodea, el cultivo de piezas de repuesto en un tejido completo puede generar células más naturales”, que luego pueden reemplazar el tejido dañado y muerto.
David Gamm, profesor y oftalmólogo pediátrico de la Universidad de Wisconsin, compara el proceso con la fabricación de repuestos para un automóvil. “Podemos fabricar bujías para su automóvil, pero si el motor está totalmente derretido y oxidado, las bujías nuevas no funcionarán”, dice. Mecánica Popular. Del mismo modo, los pacientes que han perdido sus conos o bastones pero han conservado el resto de la arquitectura neural subyacente, podrían beneficiarse de los fotorreceptores trasplantados, mientras que aquellos que están más avanzados en sus enfermedades necesitarían una mayor reconstrucción.
Su equipo recientemente coeditado investigación con el laboratorio de Raunak Sinha en la Universidad de Wisconsin-Madison, lo que demuestra que los fotorreceptores de cono en los organoides de la retina cultivados a partir de células madre humanas responden a la luz como lo hacen las retinas de los macacos. Ahora, Gamm está a punto de intentar reemplazar esta bujía en los próximos ensayos clínicos. “Hemos demostrado que la célula tiene esa capacidad para detectar la luz y que es una célula real y auténtica. Pero se puede instalar [itself in the right place] y pasar esa señal a una célula nativa en ese paciente?
Pero Gamm advierte que el progreso será gradual. “Si ha sido tetrapléjico durante 30 años, la idea de correr un maratón después de recibir la terapia con células madre no es realista”. Del mismo modo, Gamm cree que la tecnología ofrecerá mejoras pequeñas y significativas al principio, como que alguien que solo puede detectar la luz también sea capaz de detectar el movimiento. “Y luego innovaremos en eso”.