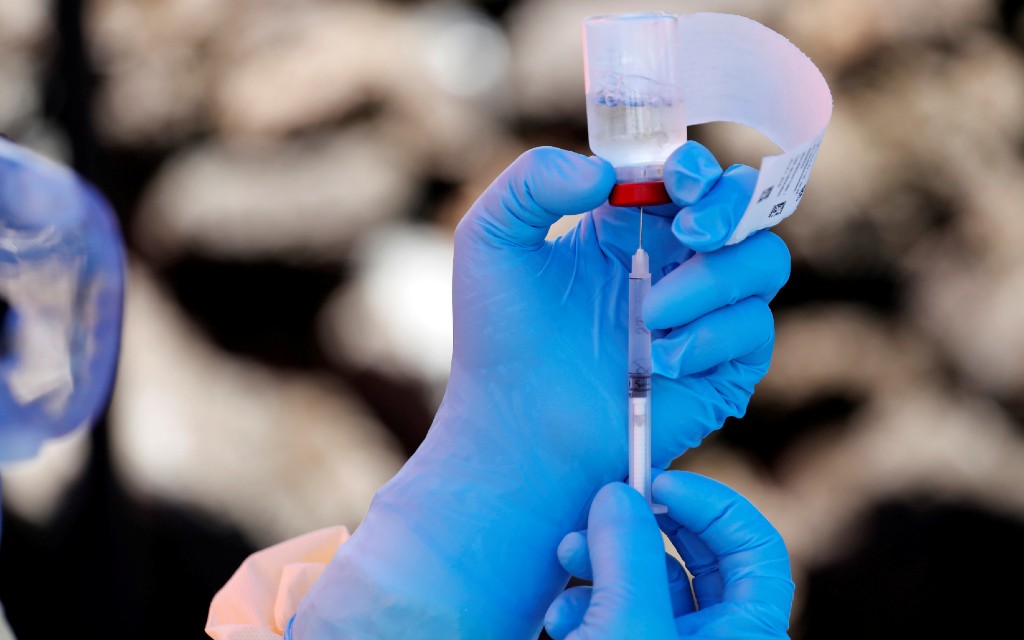
Para los expertos, lo ideal es un producto seguro en lugar de ser el primero en vacunar. Según los creadores del fármaco, más de 20 países muestran interés por adquirir Sputnik V, incluido México; pero la SRE informó que está en negociaciones con EU y China.
Al entusiasmo inicial por la vacuna anti-Covid Sputnik V anunciada por Rusia este martes, siguieron voces en contra y advertencias por parte de autoridades sanitarias y expertos en diversas disciplinas de la investigación médica.
Incluso, la Organización Mundial de la Salud (OMS) señaló que no debe sacrificarse la seguridad y eficiencia a cambio de la velocidad.
“Necesitamos seguir invirtiendo y acelerando el desarrollo de tratamientos y vacunas sanas y efectivas, que nos ayuden a reducir la transmisión y las muertes por Covid-19 en el futuro. Pero apresurar el progreso no quiere decir arriesgar la seguridad”, enfatizó este martes Tarik Jasarevic, portavoz de la OMS.
En una conferencia de prensa virtual desde Ginebra, Jasarevic se refirió al anuncio hecho por el presidente ruso Vladimir Putin de que su país desarrolló y aprobó ya una vacuna contra el coronavirus.
El proyecto de vacuna de Rusia no estaba en la lista de los seis más avanzados que mencionó la semana pasada la OMS y que incluía tres vacunas en China, dos en Estados Unidos y una de la Universidad de Oxford.
“Acelerar el desarrollo de la vacuna conlleva seguir los procesos de pruebas, manufactura y logística”, explicó Jasarevic, según un comunicado de la ONU.
La vacuna que ha registrado Rusia debe seguir todos los trámites de precalificación y revisión establecidos por la OMS, agregó.
En México, el subsecretario de Prevención y Promoción de la Salud, Hugo López-Gatell, afirmó que no debe usarse una vacuna que no haya cumplido con todos los pasos.
“Nos ha sorprendido, como le sorprendió a la OMS, conocer de la vacuna rusa cuando hasta donde llegaba la información pública mundial no habían llegado hasta la fase 3. Definitivamente, y esto quisiera dejarlo muy claro: no se puede empezar a utilizar una vacuna que no haya terminado satisfactoriamente los estudios de fase 3”, alertó el funcionario.
Durante la conferencia de prensa desde Palacio Nacional, López-Gatell afirmó que no cree que haya para uso mundial una vacuna antes del final de este 2020.
“No hay vacunas o compañías que lo hagan por filantropía y parte de la especulación comercial será anunciar que ya casi está la vacuna, y eso lleva a que aumenten los precios de las acciones de las empresas, que haya mayores ganancias”.
Lanzamiento de Sputnik V, la vacuna
“Esta mañana, fue registrada la primera vacuna contra el Covid-19 en el mundo“, informó ayer el presidente de Rusia, Vladimir Putin, en una reunión con el Gabinete de Ministros.
El mandatario aseguró que se habían completado las verificaciones necesarias y era un paso muy importante para Rusia y para el mundo entero.
Además, destacó la eficacia de la vacuna desarrollada por el Centro Nacional de Epidemiología y Microbiología Gamaleya.
Para septiembre, el Centro Gamaleya planea comenzar a producir de forma masiva la vacuna Sputnik V y, para finales de año, incrementar la producción hasta 200 millones de dosis, incluidas 30 millones para Rusia.
El principio activo de la vacuna, en que se basa la plataforma tecnológica única de la vacuna, se encuentra actualmente en proceso de obtención de una patente, que fue solicitada desde mayo.
Según la página oficial de los creadores del fármaco, más de 20 países han expresado su interés en adquirir Sputnik V, incluido México.
En su página, también aseguran que la tercera fase de ensayos clínicos comenzará este miércoles 12 de agosto con más de 2 mil participantes en Rusia y varios países de Oriente Medio y América Latina, y de nuevo menciona a México.
Sin embargo, este martes Marcelo Ebrard, secretario de Relaciones Exteriores, señaló que para la compra de vacunas México tiene entendimiento o negociaciones con tres empresas, una de Estados Unidos y dos de China, para que lleven a cabo en el país la fase 3 del protocolo clínico.
Incluso, en su conferencia matutina, el presidente Andrés Manuel López Obrador adelantó el martes que el país dispondría de un presupuesto de hasta 100 mil millones de pesos para la compra de vacunas.
Esperanza y escepticismo
Tras el anuncio de la primera vacuna, Israel dio a conocer que la examinará y entablará negociaciones para comprarla si se determina que es un “producto serio”, dijo el ministro de salud de Israel, según declaraciones retomadas por la agencia Reuters.
Científicos de Filipinas se reunieron el miércoles con los investigadores de Rusia que desarrollaron la vacuna para discutir la posible participación en ensayos clínicos y el acceso a sus datos de investigación.
Kazajstán también planea enviar funcionarios del gobierno a Moscú a finales de este mes para discutir posibles entregas, informó la agencia en un cable.
El ministro de Salud alemán, Jens Spahn, dijo que la vacuna no se había probado lo suficiente y que el objetivo era tener un producto seguro en lugar de ser el primero en comenzar a vacunar a las personas.
Génesis de la vacuna
El Fondo Ruso de Inversión Directa (RDIF) financia la producción de la vacuna Sputnik V a través de la capacidad de producción de las empresas en su cartera, R-Pharm y Binopharm, que forma parte del grupo Alium.
Según su página web del Centro Gamaleya, el fondo ve un gran interés en el mundo por la vacuna y planea realizar una tercera fase de ensayos clínicos en varios países, incluidos Arabia Saudita, Emiratos Árabes Unidos, Brasil, India y Filipinas, así como comenzar la producción en masa en varios países en asociación con fondos soberanos locales, incluidos India, Corea del Sur, Brasil. Además, se está estudiando la posibilidad de producir la vacuna en Arabia Saudita, Turquía y Cuba.
El Centro Nacional de Epidemiología y Microbiología Gamaleya, fundado en 1891 como laboratorio privado, es una institución líder en su ámbito a nivel mundial.
Desde los años 80, ha liderado los esfuerzos para desarrollar una plataforma tecnológica basada en adenovirus, que se encuentran en los adenoides humanos.
El centro desarrolló y registró con éxito, en 2015, dos vacunas contra el Ébola (una tercera fue registrada en 2020), usando la plataforma de vectores adenovirales. Desde 1997, el centro ha sido dirigido por el doctor en biología Alexander Gintsburg, miembro de la Academia Rusa de Ciencias.
De acuerdo con la página web, antes de embarcarse en los ensayos clínicos, la vacuna pasó en su totalidad todas las etapas de los ensayos preclínicos de eficacia y seguridad, que incluyeron experimentos con varios tipos de animales de laboratorio, incluidas dos especies de primates.
Los ensayos clínicos de fase 1 y 2 de la vacuna se completaron el 1 de agosto de 2020.
“Todos los voluntarios toleraron bien las pruebas, no se registraron efectos adversos graves o inesperados. La vacuna indujo la formación de una alta respuesta inmune celular y de anticuerpos”.
Ningún participante en el ensayo clínico actual ha contraído el coronavirus después de la administración de la vacuna, señala.
La vacuna recibió un certificado de registro por parte del Ministerio de Salud de la Federación Rusa apenas este martes 11 de agosto de 2020 y, de acuerdo con la legislación aprobada durante la pandemia, puede usarse ya para vacunar a la población en Rusia.
Voces en contra
La Organización Mundial de la Salud está en contacto con las autoridades sanitarias rusas, discutiendo la posible precalificación de la vacuna, con la revisión y evaluación rigurosas de los datos sobre seguridad y eficacia obtenidos mediante las pruebas, enfatizó este martes Tarik Jasarevic, portavoz del organismo internacional.
Afirmó que es alentadora la velocidad con la que se están desarrollando varias vacunas y confió en que algunas demuestren ser seguras y eficientes después de pasar por los protocolos y pruebas correspondientes.
Del mismo modo, dijo que cuando esto se consiga, la OMS podrá adquirir dosis para su distribución equitativa a los diferentes países.
Según las autoridades rusas, la vacuna podría empezar a aplicarse en septiembre y daría inmunidad por dos años a las personas inoculadas.
Al respecto, Jasarevic señaló que cada país cuanta con sus propias regulaciones y agencias sanitarias para aprobar el uso de vacunas o medicamentos en su territorio, pero que la OMS tiene establecido un proceso de precalificación.
Actualmente, la OMS tiene registrados 160 proyectos de vacunas contra el Covid-19, más de 20 de ellos en la fase de pruebas clínicas.
La Organización Panamericana de la Salud (OPS) también informó el martes que no adquirirá ninguna vacuna que no haya seguido los pasos correspondientes y obtenido la autorización de la OMS.
El doctor Jarbas Barbosa, subdirector de la agencia regional, subrayó que el desarrollo de vacunas sigue en todo el mundo un proceso estandarizado que incluye tres fases de ensayos clínicos.
“No se puede utilizar una vacuna o medicamento sin que se cumplan todas las etapas·”, recalcó.
Detalló que después de completar los ensayos clínicos en las fases 1, 2 y 3, el productor solicita la aprobación de la autoridad regulatoria de su país y de los países donde quiera comercializar su producto.
“La autoridad regulatoria analiza la calidad y revisa rigurosamente todos los datos de las pruebas clínicas porque ésta es la garantía de que una vacuna es segura y eficaz”, apuntó Barbosa.
Reiteró que la OMS está en contacto con las autoridades regulatorias rusas para recibir la información pertinente de la vacuna en cuestión.
“Para que sea recomendada y que los países puedan adquirirla por medio del Fondo Rotatorio de Vacunas de la OPS, cualquier vacuna tiene que ser precalificada por la OMS, lo cual quiere decir que la organización ha revisado la seguridad y la calidad”, puntualizó Barbosa.
Algunos expertos de salud de la comunidad internacional también expresaron su alarma, ya que Rusia aún no ha llevado adelante ensayos a gran escala que determinen si su fórmula es efectiva.
La autorización por vía rápida podría implicar que no se hayan detectado los efectos adversos que podría tener una vacuna potencial, que aunque posiblemente sean excepcionales, podrían ser graves, señaló Ayfer Ali, especialista en el desarrollo de fármacos de Warwick Business School en Reino Unido.
Mientras que Francois Balloux, experto del Instituto de Genética del University College London, calificó el anuncio como una decisión tonta, riesgosa y poco ética.
“Cualquier problema con la campaña de vacunación de Rusia podría resultar en un desastre por sus efectos negativos en la salud de personas y por la posibilidad de que la población pueda no aceptar más adelante otro tipo de la vacuna”.
Otros laboratorios han decidido esperar, como Moderna, Pfizer y AstraZeneca.
Apenas hace unos días, el director general de la Organización Mundial de la Salud , Tedros Adhanom Ghebreyesus, afirmó que, pese a los avances en el desarrollo de una vacuna contra el Covid-19, no hay una bala de plata en este momento.
“Quizá no la haya nunca”, lamentó.
El Comité de la OMS recomendó que los países participen en el Acelerador de Acceso a las Herramientas Covid-19 (ACT), también en ensayos clínicos relevantes y se preparen para una introducción terapéutica y segura de vacunas.
La organización espera tener una cantidad de vacunas efectivas que puedan ayudar a prevenir la infección de las personas.
Con información de agencias y Noticias ONU