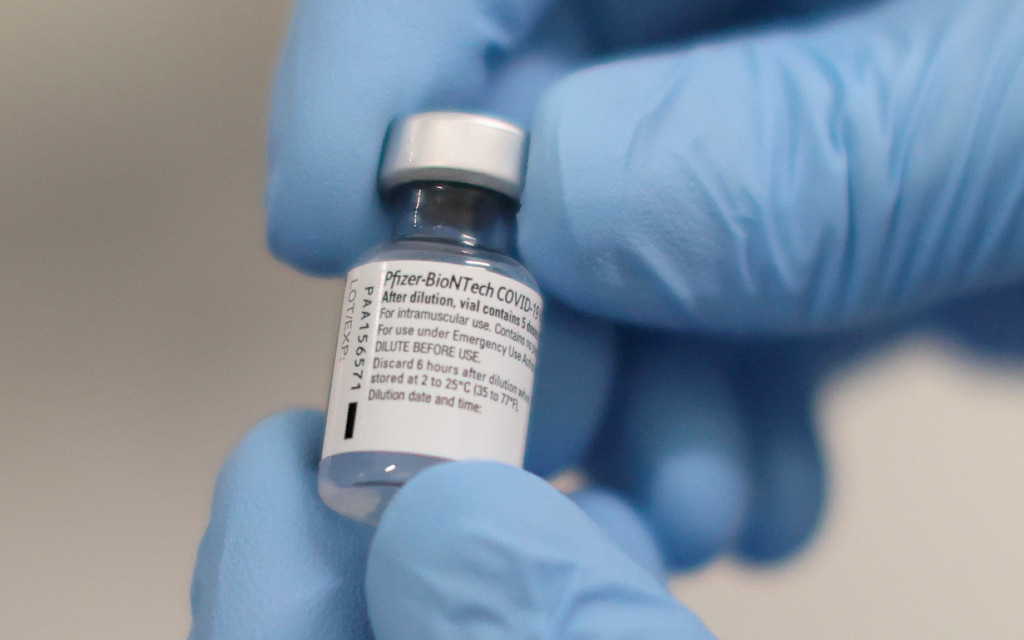
A más tardar, el organismo regulador europeo completaría para el 29 de diciembre las revisiones para la vacuna Pfizer/BioNTech y para el 12 de enero, las de Moderna.
Los datos presentados a la Agencia Europea de Medicamentos (EMA) por Pfizer/BioNTech y Moderna para sus candidatas a vacuna Covid-19 son “muy robustos”, dijo el jueves la directora ejecutiva del organismo.
“Tenemos un conjunto de datos de más de 30 mil sujetos que han sido seguidos a través de los ensayos clínicos. Esto nos da un conjunto de datos muy robusto sobre el cual tomar una decisión, tanto sobre seguridad como sobre eficacia“, dijo Emer Cooke en la reunión de un panel del Parlamento Europeo.
El 29 de diciembre, la agencia completaría las revisiones para la vacuna Pfizer/BioNTech y, para el 12 de enero, para la vacuna Moderna, “a más tardar”.
Cooke aseguró que las fechas de la decisión de aprobación podrían cambiar, dependiendo de la evaluación.
Foto: Reuters
“No podemos garantizar que habrá un resultado positivo en esta etapa”, dijo Cooke,.
Agregó que los expertos de la agencia tuvieron que examinar conjuntos de datos muy grandes.
“Tenemos que asegurarnos de analizar esos datos correctamente”.
Cooke señaló que los analistas de EMA también estaban cotejando los datos con la nueva información que surgió en Gran Bretaña el miércoles, cuando dos personas sufrieron anafilaxia y otra, una posible reacción alérgica después de que comenzó el despliegue de la vacuna de Pfizer/BioNTech.
Añadió que espera que AstraZeneca y Johnson & Johnson presenten en el primer trimestre del próximo año sus solicitudes de autorización de comercialización de sus candidatas a vacuna Covid-19.
La agencia ha estado evaluando los datos preliminares de AstraZeneca desde inicios de octubre y los de Johnson & Johnson desde principios de diciembre.
Con información de Rts