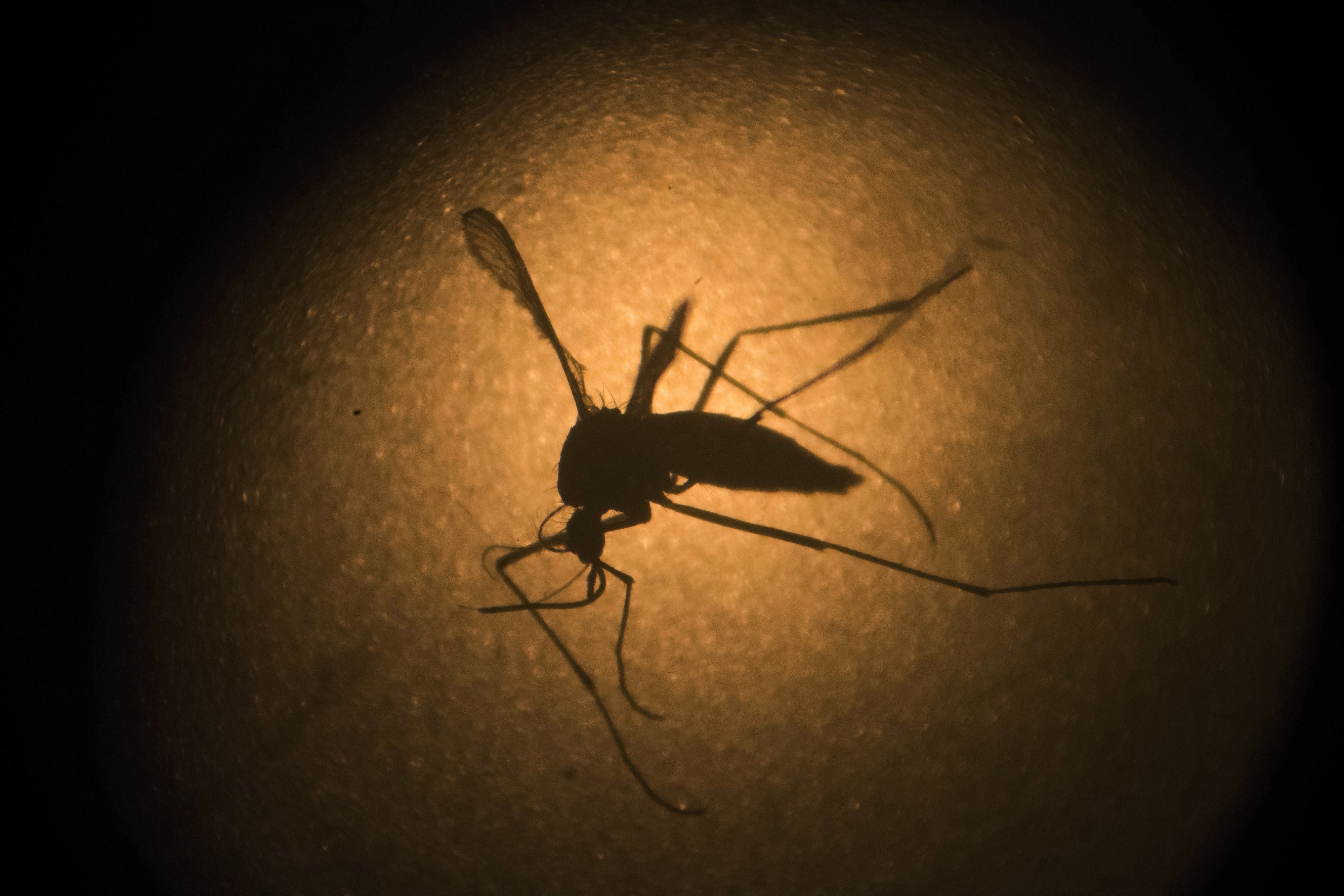
Desde hace unos años, una empresa originada en los laboratorios de la Universidad de Oxford crea seres vivos con capacidades que hasta ahora no existían en la naturaleza. Su primera criatura fue una variante del mosquito Aedes aegypti que llevaba insertado en su genoma ADN de coral marino, bacterias, moscas y polillas. El objetivo de esas modificaciones era sencillo: crear mosquitos machos capaces de aparearse con las hembras para pasar a su descendencia una herencia genética que garantiza que ninguno de sus hijos sobrevivirá.
Así dicho puede parecer algo terrible, pero las hembras de Aedes aegypti son las responsables de transmitir enfermedades que afectan a millones de personas, como el dengue, el zika y el chikungunya. En diferentes experimentos en Brasil, los creadores de estos mosquitos diseñados para eliminar a su propia estirpe demostraron que reducen la incidencia del dengue hasta en un 90%. La compañía, Oxitec, ya está probando en Brasil una segunda generación de mosquitos transgénicos que producen solo machos; incapaces de picar y de transmitir enfermedades. También está desarrollando una nueva variante para intentar esterilizar al mosquito que transmite la malaria, una enfermedad que sufren más de 200 millones de personas en todo el mundo y que cada año mata a más de 400.000, la mayoría niños.
Hoy se publican los resultados del primer experimento en campo abierto con otra de las creaciones de esta compañía biotecnológica. Se trata de una variante de la polilla Plutella xylostella que es una de las peores plagas agrícolas del mundo. Las larvas de este insecto se alimentan de cultivos como el brécol, el repollo o la coliflor y causan cada año pérdidas de unos 4.000 millones de euros. Lo peor de esta polilla es que se ha vuelto resistente a la mayoría de los insecticidas.
“Este insecto es el líder mundial en resistencia a los insecticidas”, explica Tony Shelton, entomólogo de la Universidad de Cornell (EE UU). “Esta es una de las peores plagas agrícolas de todo el mundo especialmente en zonas cálidas, como el sur de EE UU, Asia, incluidas China, India y Tailandia, así como España e Italia”, resalta.
Larvas de la polilla ‘xylostella’ devorando hojas de repollo.
Aquí es donde entra en juego la polilla OX4318L, una variante modificada cuyo genoma lleva pequeños fragmentos sintéticos inspirados en los de otros organismos, incluidos los ya mencionados más otros nuevos, como el virus del herpes. Estas modificaciones hacen que los machos transgénicos les pasen a las hembras un legado genético que las hace adictas a la tetraciclina, un antibiótico. Sin ese compuesto las larvas mueren a los pocos días. Este truco permite a los investigadores criar en el laboratorio generaciones de la polilla usando ese antibiótico y les asegura de que toda la progenie morirá en los campos sin causar daños.
El equipo de Shelton junto a expertos de Oxitec ha realizado la primera suelta de estas polillas modificadas que se ha hecho en campo abierto: un cultivo de repollos debidamente aislado en Geneva, en el estado de Nueva York. Los resultados, publicados hoy en Frontiers in Bioengineering and Biotechnology, demuestran que los machos modificados genéticamente se comportan igual que los salvajes y que se aparean con las hembras con toda normalidad.
Los investigadores liberaron casi 10.000 polillas salvajes y otras 10.000 modificadas, lo que ha servido para recapturar algunas de ellas después de unos días con trampas que despiden feromonas. El trabajo muestra que la mayoría de los insectos apenas viajan unas decenas de metros desde su punto de suelta. Ningún ejemplar transgénico apareció en las trampas situadas fuera del campo experimental, un buen dato en relación con la seguridad para un futuro uso comercial. “Estudios previos hechos en invernaderos han demostrado que las polillas transgénicas reducen drásticamente esta plaga en apenas dos generaciones [un mes]”, explica Shelton. “Creo que va a haber varias formas de usar esta tecnología, la primera, anteponerse a la plaga y soltar polillas modificadas de forma profiláctica y la segunda, liberar una población más grande de insectos modificados para eliminar una plaga que ya está asentada”, detalla.
Esta táctica no es completamente nueva. Desde los años 50 se han creado poblaciones enteras de mosquitos estériles para acabar con plagas, pero se hace bombardeando a los machos con radiación. Esta táctica permitió eliminar el gusano barrenador del ganado en América del Norte, México y zonas de África. “Lo malo de esta táctica es que es como pegarles a los machos con un martillo en la cabeza, les vuelve menos competentes que los machos salvajes”, explica Shelton, que añade que la modificación genética es mucho más “específica” y permite además usar menos insecticidas, lo que tiene beneficios ambientales.
“Nuestro objetivo ahora es hacer más sueltas experimentales en cultivos para comprobar que la medida es segura y que funciona”, explica Neil Morrison, jefe de programas agrícolas de Oxitec y coautor del estudio. “Creemos que esta puede ser una nueva herramienta para evitar estas plagas y evitar la aparición de especies resistentes a insecticidas”, resalta. La polilla empleada en EE UU sería solo la primera de sus criaturas dedicadas a la extinción de pestes, a la que luego seguirían otras especies, como la mosca mediterránea de la fruta o la del olivo, que la empresa ya intentó probar en un campo español en 2015, aunque el experimento no llegó a llevarse a cabo, explica Morrison. “Aún somos una empresa pequeña y tenemos que ir paso a paso, con lo que ese proyecto por ahora debe esperar”, explica.
Organizaciones ecologistas se oponen a este tipo de experimentos. Argumentan que puede contaminar y arruinar la certificación de los cultivos orgánicos adyacentes. También consideran que se debería demostrar que las larvas muertas de esta polilla son inofensivas para los animales o personas que se las puedan comer.
La entomóloga Dolors Piulachs opina que es “un estudio muy completo que demuestra que sería efectivo como medida de control de plagas”, aunque sería solo un arma más para el arsenal y no funcionará con todas las plagas. Esta investigadora del Instituto de Biología Evolutiva (CSIC-UPF) piensa que “no hay posibilidad de que los genes de la especie modificada permanezcan presentes, pues todas las hembras mueren”. “Cualquier animal que se coma a una de las larvas muertas o a un mosquito macho no tendría ningún problema pues el ADN quedaría degradado en el sistema digestivo”, resalta. “Hay que recordar que no se trata aquí de erradicar una especie, pues siempre quedarán ejemplares salvajes en algún rincón, solo se trata de sacarlos de los cultivos, porque lo más importante es que la gente pueda comer y que se usen menos pesticidas”, resalta. “El único problema que puede tener esta táctica es que al reducir o eliminar una especie aparezca otra plaga que aproveche el hueco”, añade.
