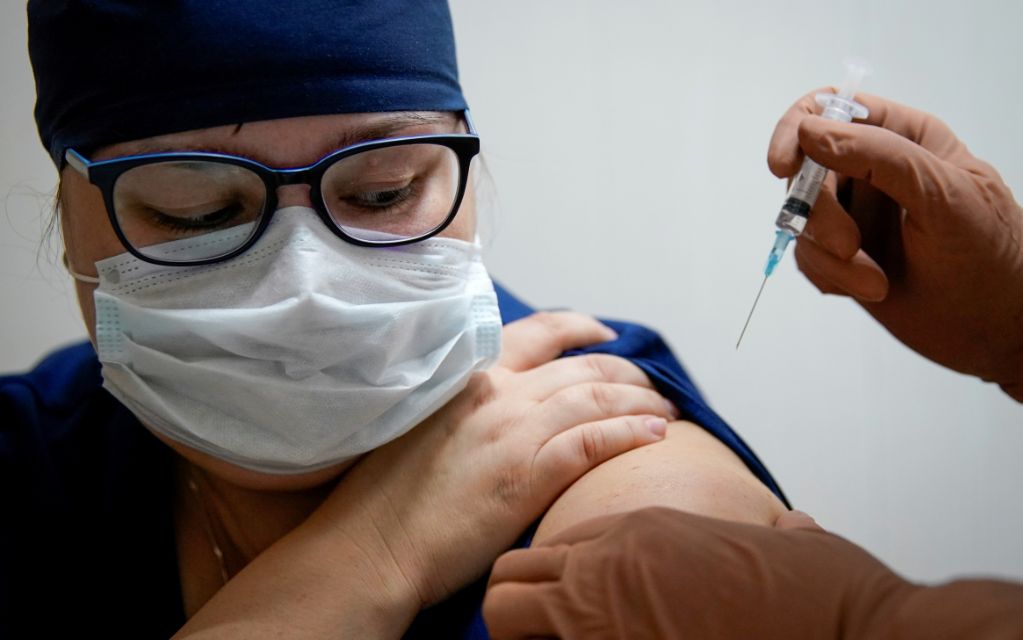
Es importante comprender qué hay detrás de los anuncios de pruebas de vacunas candidatas, que no nos dicen las noticias y qué es lo que los investigadores aún no saben.
Las últimas semanas se han difundido noticias sobre las vacunas contra el coronavirus. Primero escuchamos los resultados preliminares de los ensayos clínicos de la vacuna Pfizer, luego sobre la vacuna rusa Sputnik V. Esta semana, escuchamos sobre la vacuna Moderna. Todos estos resultados se compartieron con los medios, antes de ser sometidos a revisión por pares y de ser publicados en revistas de divulgación científica.
Conforme esperamos la publicación de los resultados preliminares de más ensayos de vacunas en las próximas semanas y meses, es importante comprender qué hay detrás de los anuncios de pruebas de vacunas candidatas, que no nos dicen las noticias y qué es lo que los investigadores aún no saben.
Esto puede ayudarnos a identificar buenas noticias cuando las vemos, a ser más críticos con los informes o tener cautela en nuestro juicio hasta que tengamos más información.
En esta etapa de la pandemia, los resultados de los ensayos que aparecen en los titulares son generalmente los resultados provisionales de los ensayos clínicos en etapa tardía, conocidos como fase 3. Esto es cuando una vacuna se administra a miles de personas y se prueba para ver qué tan bien funciona y si es seguro.
En estos ensayos, los voluntarios se asignan al azar en dos grupos de estudio, el grupo de la vacuna (personas que reciben la vacuna real) y el grupo de placebo (personas que reciben el placebo, generalmente una sustancia inerte, como una inyección de solución salina). Sin embargo, algunos ensayos de vacunas utilizan vacunas contra otras enfermedades como placebo.
Entonces, idealmente, los informes de los medios deberían mencionar cómo se comparan los resultados de la vacuna con el placebo o la vacuna de comparación.
Antes de que la vacuna llegue a esta etapa, habrá completado con éxito ensayos más pequeños (fase 1 y 2). A menudo, las fases de los ensayos clínicos se combinan. Por lo tanto, podría obtener resultados de un ensayo que combine las fases 1 y 2, o las fases 2 y 3.
Como las vacunas se prueban principalmente en voluntarios sanos, es extremadamente importante demostrar que la vacuna es segura.
Los efectos secundarios (también llamados eventos adversos) se informan a un comité independiente, generalmente con dos o más expertos en inmunología y medicina, así como un bioestadístico.
Una de las funciones de este comité de monitoreo de datos es recibir y examinar informes de eventos adversos y observar los resultados provisionales para determinar si el ensayo debe continuar.
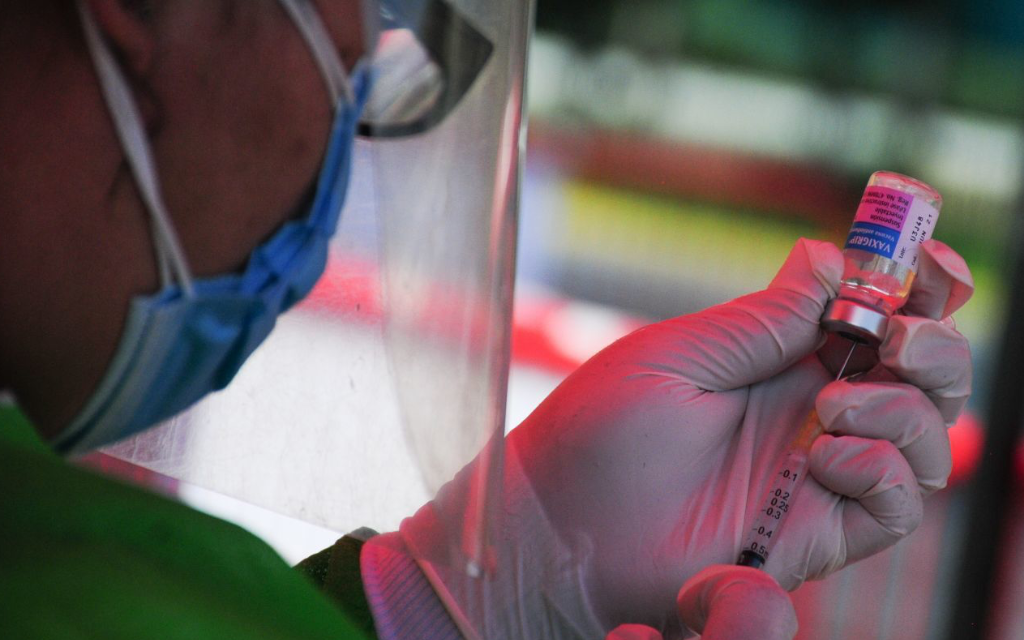
En ocasiones, si se plantean problemas de seguridad, un ensayo se detiene temporalmente mientras el comité investiga. Esto es lo que sucedió con el ensayo de la vacuna de la Universidad de Oxford/AstraZeneca, que desde entonces se ha reiniciado.
Por lo tanto, cualquier informe de los medios debe mencionar cuántas personas se ven afectadas por los efectos secundarios, el tipo de efectos secundarios (comunes / raros, graves / leves), si ocurrieron en personas en el brazo de la vacuna o placebo del ensayo, y si los datos de monitoreo El comité está investigando. No todos estos detalles están disponibles para el público.
Los resultados del ensayo se miden en uno o más puntos temporales intermedios y al final del ensayo. Este es otro factor que supervisa el comité de seguimiento de datos.
Por ejemplo, el comité tiene reglas sobre la eficacia de la vacuna que se aplica a la mitad del ensayo para determinar si el ensayo continúa. Por tanto, una regla podría ser algo como “Para que el ensayo continúe, la eficacia de la vacuna debe ser al menos del 60% después de que el 25% de los sujetos hayan completado el ensayo”.
Los tipos de resultados que aparecen en los titulares actualmente provienen de este tipo de análisis intermedio. En otras palabras, el comité habrá evaluado los resultados hasta el momento y habrá dado luz verde al ensayo para continuar.
Ningún ensayo clínico de fase 3 ha informado aún el análisis completo de decenas de miles de participantes del estudio, pero esto sucederá en las próximas semanas.

Eficacia de la vacuna
La eficacia de la vacuna describe qué tan bien ofrece la vacuna contra la enfermedad objetivo. Las fórmulas y los cálculos pueden volverse bastante complicados, por lo que solo daré un ejemplo simple aquí.
Una medida se basa en la “tasa de ataque”, que es la proporción de personas en el ensayo diagnosticadas con Covid-19. Medimos la tasa de ataque en el brazo de la vacuna y el brazo de placebo por separado, luego dividimos uno por el otro para obtener la “tasa de tasa de ataque”. Luego restamos el índice de tasa de ataque de 1 para obtener una medida de la eficacia de la vacuna.
Por ejemplo, si se diagnostica Covid-19 al 5% del brazo de la vacuna, mientras que se diagnostica el 40% del placebo, entonces la tasa de ataque es (5% / 40%) o 0,125 o 12,5%. Eso da una eficacia de la vacuna del 87,5% (100% – 12,5%).
Respuesta inmune
Algunos ensayos de vacunas informan qué tan bien responde el sistema inmunológico (inmunogenicidad). Por ejemplo, el ensayo de la Universidad de Oxford / AstraZeneca ha informado de la respuesta de anticuerpos, así como de varias otras medidas de inmunogenicidad.
Algunos ensayos sólo informan sobre la inmunogenicidad. Esto permite que el ensayo sea más pequeño, más corto y menos costoso que los ensayos de eficacia de la vacuna, ya que utilizan la inmunogenicidad como sustituto de la eficacia de la vacuna.
Aunque la eficacia es el criterio de valoración preferido para los ensayos de vacunas, algunas autoridades reguladoras aceptan pruebas de inmunogenicidad para autorizar una vacuna.
Efectividad de la vacuna
La eficacia de la vacuna describe qué tan bien ofrece la vacuna contra la enfermedad objetivo en el mundo real, en lugar de en un ensayo clínico controlado. Los ensayos de vacunas generalmente incluyen voluntarios sanos, pero a menudo no nos dicen qué tan bien funciona la vacuna en niños, ancianos o personas con sistemas inmunológicos comprometidos.
La eficacia de la vacuna informada del 90-95%, como hemos escuchado recientemente, puede sonar impresionante. Sin embargo, en las condiciones del mundo real, es probable que las vacunas ofrezcan mucha menos protección en algunos grupos de población.
Los ensayos actuales informan si una vacuna previene o no Covid-19 (en otras palabras, los síntomas), no si previene la infección en sí. Sin embargo, un informe reciente de los medios sobre la vacuna Pfizer dice que es probable que prevenga el 50% de las infecciones, así como el 90% de los sintomáticos Covid-19.
Si la vacuna tiene una eficacia del 90%, entonces el 10% de las personas vacunadas aún podrían contraer la enfermedad sintomática. Esperamos que estas personas tengan una enfermedad mucho más leve, pero no sabemos si este es el caso.
Tampoco sabemos cuánto tiempo dura la inmunidad o si hay efectos secundarios a largo plazo. Todo lo que podemos hacer ahora es esperar con paciencia a que lleguen los resultados completos de la prueba de fase 3 durante las próximas semanas. (Rts)